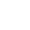Definition af pH-meter
Et pH-meter refererer til et instrument, der bruges til at bestemme pH-værdien af en opløsning. pH-meteret fungerer efter princippet om et galvanisk batteri. Den elektromotoriske kraft mellem de to elektroder i det galvaniske batteri er baseret på Nerns lov, som ikke kun er relateret til elektrodernes egenskaber, men også til koncentrationen af hydrogenioner i opløsningen. Der er et tilsvarende forhold mellem den elektromotoriske kraft i det primære batteri og hydrogenionkoncentrationen, og den negative logaritme af hydrogenionkoncentrationen er pH-værdien. pH-meteret er et almindeligt analyseinstrument, der er meget anvendt i landbrug, miljøbeskyttelse og industri. Jordens pH er en af de vigtige grundlæggende egenskaber ved jorden. Faktorer som temperatur og ionstyrke i den opløsning, der skal testes, bør tages i betragtning under pH-målingen.
Princippet for pH-måleren
pH defineres som den negative logaritme af hydrogenionkoncentrationen i den vandige opløsning. Selvom dette lyder kompliceret, er pH meget enkelt sagt et tal, der bruges til at kvantificere en opløsnings surhedsgrad eller alkalinitet. Tallet angiver antallet af hydrogenioner, som et specifikt stof kan frigive i opløsningen. I pH-området betragtes en pH på 7 som neutral. Opløsninger med en pH på 0-7 betragtes som sure, og opløsninger over 7 til 14 kaldes alkaliske opløsninger. I biologiske systemer er pH kritisk. Takket være den omhyggeligt justerede pH kan de fleste biomolekyler i vores krop udføre fremragende funktioner. Selv i et eksperimentelt system skal den nødvendige pH opretholdes for at opnå nøjagtige resultater. Derfor bruges en enhed kaldet et pH-meter i biologiske eksperimenter til omhyggeligt at overvåge pH.
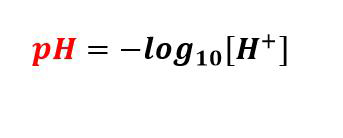
pH-meteret er en pH-responsiv elektrode, der måler aktiviteten af hydrogenioner i en opløsning og transmitterer denne information. Apparatet består af to glasrør, der hver indeholder en elektrode, en referenceelektrode og en sensorelektrode. Referenceelektroden er lavet af en mættet KCl-opløsning, mens sensorelektroden indeholder en bufferopløsning med en pH-værdi på 7, og sølvtråden belagt med sølvchlorid er nedsænket i disse to opløsninger. For enden af sensorelektroden er der en pære lavet af porøst glas belagt med silica og metalsalt.
For at måle opløsningens pH-værdi nedsænkes pH-meteret i opløsningen. Når sensorelektrodens pære er i kontakt med opløsningen, vil hydrogenionerne i opløsningen erstatte metalionerne på pæren. Denne udskiftning af metalioner får strøm til at flyde i metaltråden, som aflæses af et voltmeter.
pH-meteret er et af de mest anvendte udstyr i biologiske laboratorier. Analysér rutinemæssigt pH-værdien af buffere, opløsninger og reagenser for at sikre, at de eksperimentelle betingelser er korrekte. For at sikre nøjagtige aflæsninger skal udstyret kalibreres regelmæssigt.
Anvendelse af pH-målerdetektor
Anvendelse af pH-målerdetektor i husholdningsspildevandsbehandlingsprocesser

Anvendelse af pH-meter i galvanisering af spildevandsbehandling

Anvendelse af online pH-måler i industrien

Kalibrering af pH-måler
Opslagstidspunkt: 15. dec. 2021